Východiskový materiál: RNA
Kvantitatívna reverzná transkripčná PCR (RT-qPCR) je experimentálna metóda používaná v PCR experimentoch s použitím RNA ako východiskového materiálu.Pri tejto metóde sa celková RNA alebo mediátorová RNA (mRNA) najprv prepíše do komplementárnej DNA (cDNA) pomocou reverznej transkriptázy.Následne sa uskutočnila qPCR reakcia s použitím cDNA ako templátu.RT-qPCR sa používa v rôznych aplikáciách molekulárnej biológie, vrátane analýzy génovej expresie, validácie RNA interferencií, mikročipovej validácie, detekcie patogénov, genetického testovania a výskumu chorôb.
Jednokrokové a dvojkrokové metódy pre RT-qPCR
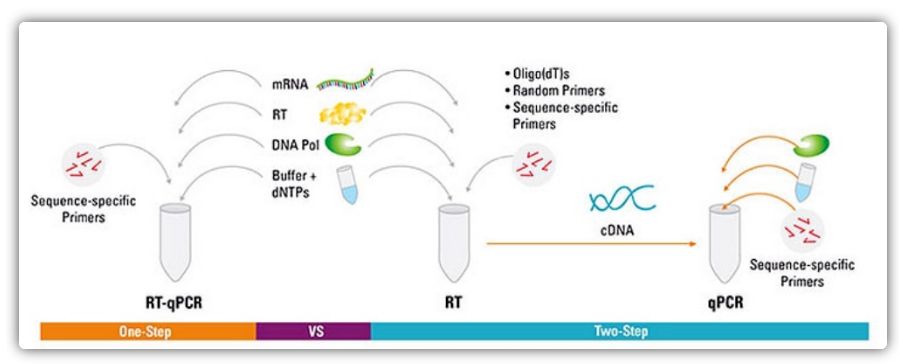
RT-qPCR sa môže uskutočniť jednokrokovou alebo dvojkrokovou metódou.Jednokroková RT-qPCR kombinuje reverznú transkripciu a PCR amplifikáciu, čo umožňuje reverznej transkriptáze a DNA polymeráze dokončiť reakciu v rovnakej skúmavke za rovnakých podmienok pufra.Jednokroková RT-qPCR vyžaduje len použitie sekvenčne špecifických primérov.V dvojkrokovej RT-qPCR sa reverzná transkripcia a PCR amplifikácia uskutočňujú v dvoch skúmavkách s použitím rôznych optimalizovaných pufrov, reakčných podmienok a stratégií návrhu primérov.
| Výhoda | Nevýhoda | |
| Jeden krok | Táto metóda má menšiu experimentálnu chybu, pretože obe reakcie sa uskutočňujú v jednej skúmavke
Menej pipetovacích krokov znižuje riziko kontaminácie
Vhodné pre vysokovýkonnú amplifikáciu/screening, rýchle a reprodukovateľné | Dvojstupňové reakcie nie je možné optimalizovať samostatne
Keďže reakčné podmienky sú ohrozené kombináciou dvojkrokovej reakcie, citlivosť nie je taká dobrá ako pri dvojkrokovej metóde
Počet cieľov detekovaných jednou vzorkou je malý |
| Dva kroky | Schopnosť vytvárať stabilné cDNA knižnice, ktoré môžu byť skladované po dlhú dobu a použité vo viacerých reakciách
Cieľové gény a referenčné gény môžu byť amplifikované z rovnakej cDNA knižnice bez potreby viacerých cDNA knižníc
Reakčné pufre a reakčné podmienky, ktoré umožňujú optimalizáciu jednotlivých reakcií
Flexibilný výber spúšťacích podmienok | Použitie viacerých skúmaviek a viac krokov pipetovania zvyšuje riziko kontaminácie DNA, a časovo náročné.
Vyžaduje viac optimalizácie ako jednokroková metóda |
Súvisiace produkty:
RT-qPCR Easyᵀᴹ (One Step)-SYBR Green I
RT-qPCR Easyᵀᴹ (One Step)-Taqman
RT Easyᵀᴹ I Master Premix pre syntézu prvého vlákna CDNA
Real Time PCR Easyᵀᴹ-SYBR Green I Kit
Výber celkovej RNA a mRNA
Pri navrhovaní experimentu RT-qPCR je dôležité rozhodnúť, či použiť celkovú RNA alebo purifikovanú mRNA ako templát pre reverznú transkripciu.Hoci mRNA môže byť schopná poskytnúť mierne vyššiu citlivosť, celková RNA sa stále často používa.Dôvodom je, že celková RNA má ako východiskový materiál dôležitejšiu výhodu ako mRNA.Po prvé, proces vyžaduje menej purifikačných krokov, čo zaisťuje lepšiu kvantitatívnu obnovu templátu a lepšiu normalizáciu výsledkov na počiatočný počet buniek.Po druhé, vyhýba sa kroku obohatenia mRNA, čo môže zabrániť možnosti skreslených výsledkov v dôsledku rôznych výťažkov rôznych mRNA.Celkovo, keďže vo väčšine aplikácií je relatívna kvantifikácia cieľového génu dôležitejšia ako absolútna citlivosť detekcie, celková RNA je vo väčšine prípadov vhodnejšia.
Primér reverznej transkripcie
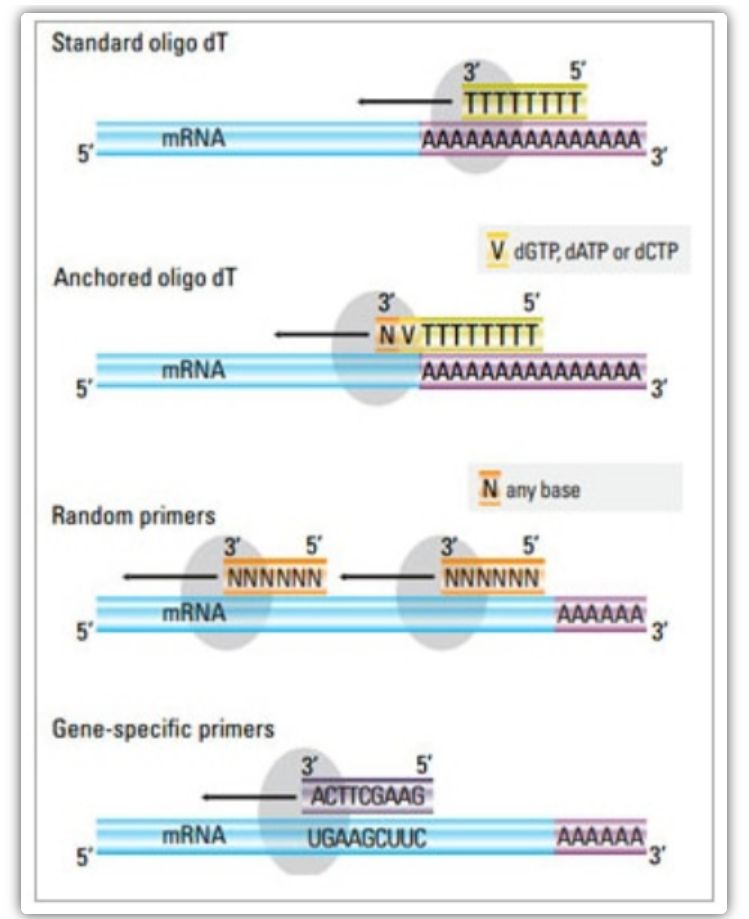
V dvojkrokovej metóde možno na aktiváciu cDNA reakcie použiť tri rôzne metódy: oligo(dT) priméry, náhodné priméry alebo sekvenčne špecifické priméry.Typicky sa oligo(dT) priméry a náhodné priméry používajú v kombinácii.Tieto priméry anelujú na vlákno templátovej mRNA a poskytujú reverznú transkriptázu s východiskovým bodom pre syntézu.
| Výber základného náteru | Štruktúra a funkcia | Výhoda | Nevýhoda |
| Oligo(dT) primer (alebo ukotvený oligo(dT) primer) | Predĺžené napojenie na tymínové zvyšky na poly(A) konci mRNA;kotviaci oligo(dT) primer obsahuje G, C alebo A na 3' konci (miesto kotvy) | Syntéza kompletnej cDNA z poly(A)-koncovej mRNA
Použiteľné, keď je k dispozícii menej východiskového materiálu
Kotviace miesto zaisťuje, že oligo(dT) primér sa viaže na 5' poly(A) chvost mRNA | Vhodné len na amplifikáciu génov s poly(A) chvostmi
Získajte cDNA skrátenú z primárneho miesta*2 v poly(A)
Predpojaté tak, aby sa viazalo na 3′ koniec*
*Táto možnosť je minimalizovaná, ak sa použijú ukotvené oligo(dT) priméry |
| náhodný základný náter
| 6 až 9 báz na dĺžku, ktoré môžu počas transkripcie RNA anelovať na viaceré miesta | Napojenie na všetky RNA (tRNA, rRNA a mRNA)
Vhodné pre transkripty s výraznou sekundárnou štruktúrou, alebo keď je k dispozícii menej východiskového materiálu
Vysoký výťažok cDNA | cDNA je reverzne transkribovaná zo všetkej RNA, čo zvyčajne nie je žiaduce a môže riediť signál cieľovej mRNA
získať skrátenú cDNA |
| sekvenčne špecifické priméry | Vlastné priméry zacielené na špecifické sekvencie mRNA | špecifická cDNA knižnica
Zlepšite citlivosť
Použitie primérov reverznej qPCR | Obmedzené iba na syntézu jedného cieľového génu |
Reverzná transkriptáza
Reverzná transkriptáza je enzým, ktorý využíva RNA na syntézu DNA.Niektoré reverzné transkriptázy majú RNázovú aktivitu a môžu po transkripcii degradovať vlákna RNA v hybridných vláknach RNA-DNA.Ak nemá enzymatickú aktivitu RNázy, môže sa pridať RNázaH pre vyššiu účinnosť qPCR.Bežne používané enzýmy zahŕňajú reverznú transkriptázu vírusu myšacej leukémie Moloney a reverznú transkriptázu vírusu vtáčieho myeloblastómu.Pre RT-qPCR je ideálne zvoliť reverznú transkriptázu s vyššou termostabilitou, aby sa syntéza cDNA mohla vykonávať pri vyšších teplotách, čím sa zabezpečí úspešná transkripcia RNA s vyššou sekundárnou štruktúrou, pri zachovaní ich plnej aktivity počas celej reakcie, výsledkom čoho sú vyššie výťažky cDNA.
Súvisiace produkty:
Foreasy M-MLV reverzná transkriptáza
Aktivita RNázy H reverznej transkriptázy
RNázaH je schopná degradovať vlákna RNA z duplexov RNA-DNA, čo umožňuje účinnú syntézu dvojvláknovej DNA.Avšak pri použití dlhej mRNA ako templátu môže byť RNA predčasne degradovaná, čo vedie k skrátenej cDNA.Preto je často výhodné minimalizovať aktivitu RNázyH počas klonovania cDNA, ak sa požaduje syntéza dlhých transkriptov.Naopak, reverzné transkriptázy s aktivitou RNázy H sú často prospešné pre aplikácie qPCR, pretože zvyšujú topenie duplexov RNA-DNA počas prvého cyklu PCR.
Návrh základného náteru
PCR priméry používané pre krok qPCR v RT-qPCR by mali byť ideálne navrhnuté tak, aby pokrývali spojenie exón-exón, kde by amplifikačný primér mohol potenciálne preklenúť skutočnú hranicu exón-intrón.Pretože sekvencie genómovej DNA obsahujúce intrón nie sú amplifikované, tento dizajn znižuje riziko falošne pozitívnych amplifikácií z kontaminujúcej genómovej DNA.
Ak nie je možné navrhnúť priméry na oddelenie exónov alebo hraníc exón-exón, môže byť potrebné ošetriť vzorky RNA DNázou I bez RNázy alebo dsDNázou, aby sa odstránila kontaminácia genómovou DNA.
RT-qPCR kontrola
Do všetkých experimentov RT-qPCR by mala byť zahrnutá negatívna kontrola reverznej transkripcie (kontrola -RT), aby sa zistila kontaminácia DNA (napríklad genómová DNA alebo produkty PCR z predchádzajúcich reakcií).Táto kontrola obsahuje všetky reakčné zložky okrem reverznej transkriptázy.Keďže pri tejto kontrole nedochádza k reverznej transkripcii, ak je pozorovaná PCR amplifikácia, je najpravdepodobnejšia kontaminácia z DNA.
Čas odoslania: august-02-2022








