Čo je mRNA vakcína
Vakcína mRNA prenáša RNA do buniek tela, aby exprimovala a produkovala proteínové antigény po príslušných modifikáciách in vitro, čím vedie telo k vytvoreniu imunitnej odpovede proti antigénu, čím sa rozširuje imunitná kapacita tela.[1,3].
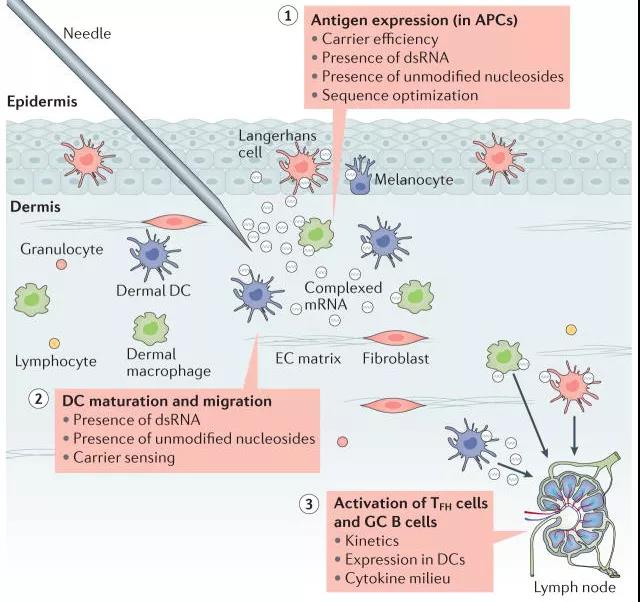
Obrázok 1: Schematický diagram účinku priamej injekcie mRNA vakcíny [2]
Klasifikácia mRNA vakcín
mRNA vakcíny sú rozdelené do dvoch typov:nereplikujúce samRNA asamozosilňujúcemRNA: samoamplifikujúca sa mRNA nielen kóduje cieľový antigén, ale kóduje aj replikáciu, ktorá umožňuje intracelulárnu amplifikáciu RNA a mechanizmus expresie proteínov.Nereplikujúce sa mRNA vakcíny kódujú iba cieľové antigény a obsahujú 5' a 3' nepreložené oblasti (UTR).Poskytujú komplexnú stimuláciu adaptability a vrodenej imunity, konkrétne in situ expresiu antigénu a prenos nebezpečného signálu, a majú nasledujúce aplikácie Vlastnosti[2,3]
●Môže poskytnúť komplexnú stimuláciu adaptability a vrodenej imunity, konkrétne in situ expresiu antigénu a prenos nebezpečného signálu
●Môže vyvolať "vyváženú" imunitnú odpoveď, vrátane humorálnych a bunkových efektorov a imunitnej pamäte
●Môže kombinovať rôzne antigény bez zvýšenia zložitosti zloženia vakcíny
●Nepretržité zlepšovanie imunitného potenciálu možno dosiahnuť opakovanou vakcináciou a imunitná odpoveď na nosič nie je žiadna alebo len malá
●Tepelne stabilné mRNA vakcíny môžu zjednodušiť prepravu a skladovanie vakcín
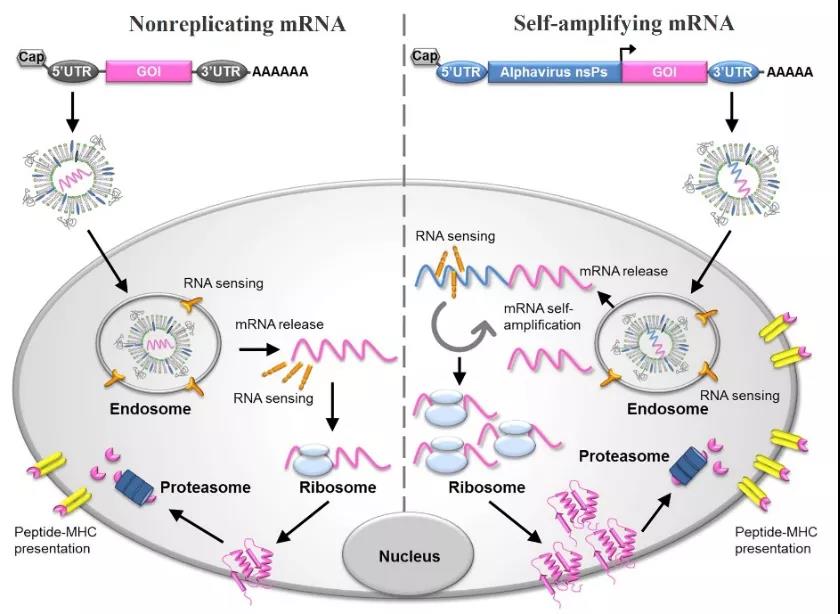
Obrázok 2: Schematický diagram mRNA vakcíny a jej mechanizmu expresie antigénu [4]
Vlastnosti mRNA vakcín
V porovnaní s tradičnými vakcínami majú mRNA vakcíny jednoduché výrobné procesy, rýchle rýchlosti vývoja, nie sú potrebné bunkové kultúry a nízke náklady.V porovnaní s DNA vakcínami mRNA vakcíny nemusia vstúpiť do jadra a neexistuje riziko integrácie do hostiteľského genómu.Polčas je možné upraviť úpravou.
Tabuľka 1: Výhody a nevýhody mRNA vakcín
|
| Výhoda | Nedostatok |
| mRNA vakcína | Rýchly výskum a vývoj, výroba vakcín trvá len 40 dní | Spustite zbytočnú imunitnú odpoveď
|
| nestabilita mRNA za fyziologických podmienok, ľahko degradovateľná | Neintegruje sa do genómu, aby sa predišlo možným terapeutickým mutáciám
| |
| Nie je potrebný žiadny jadrový lokalizačný signál, transkripcia | Efektívnosť bezpečnostnej jadrovej energie sa ešte musí overiť
|
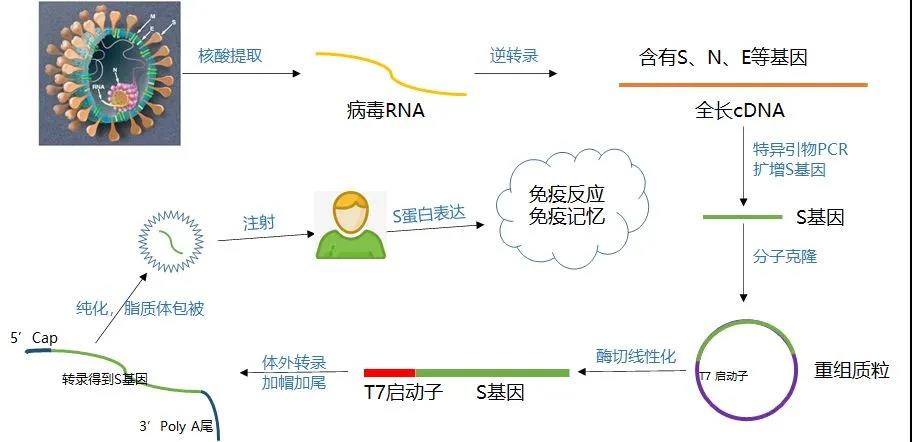
Obrázok 3: Vývojový diagram výroby a prípravy mRNA vakcíny [4]
Foregene Viral RNA Isolation kit
RT-qPCR Easy (jeden krok)
Vylepšené stratégie na prípravu mRNA vakcín
Kvôli zlej stabilite samotnej mRNA, ľahkej degradácii nukleázami v tkanivách, nízkej účinnosti vstupu do buniek a nízkej účinnosti translácie tieto defekty obmedzujú aplikáciu mRNA vakcín.Veľmi dôležitú úlohu zohráva aj účinnosť prekladu.Dodávacie vehikulá možno rozdeliť na vírusové vektory a nevírusové vektory (vrátane lipozómov, nelipozómov, vírusov, nanočastíc atď.).Preto sú potrebné príslušné opatrenia na zlepšenie.Nasleduje stratégia farmakologického zlepšenia prípravy mRNA[2]
1 Syntetizujte čiapočkové analógy alebo použite čiapočkové enzýmy na stabilizáciu mRNA a zvýšenie proteínovej translácie väzbou na eukaryotický translačný iniciačný faktor 4E (EIF4E)
2 Upravte prvky v 5′-netranslatovanej oblasti (UTR) a 3′-UTR, aby ste stabilizovali mRNA a zvýšili transláciu proteínov
3 Pridanie Poly(A) chvosta môže stabilizovať mRNA a zvýšiť transláciu proteínu
4 Modifikované nukleozidy na zníženie aktivácie vrodenej imunity a zvýšenie translácie
5 Ošetrenie RNázou III a purifikácia rýchlou proteínovou kvapalinovou chromatografiou (FPLC) môže znížiť imunitnú aktiváciu a zvýšiť transláciu
6 Optimalizujte sekvencie alebo kodóny na zvýšenie translácie
7 Spoločné dodávanie faktorov iniciácie translácie a iných metód na zmenu translácie a imunogenicity
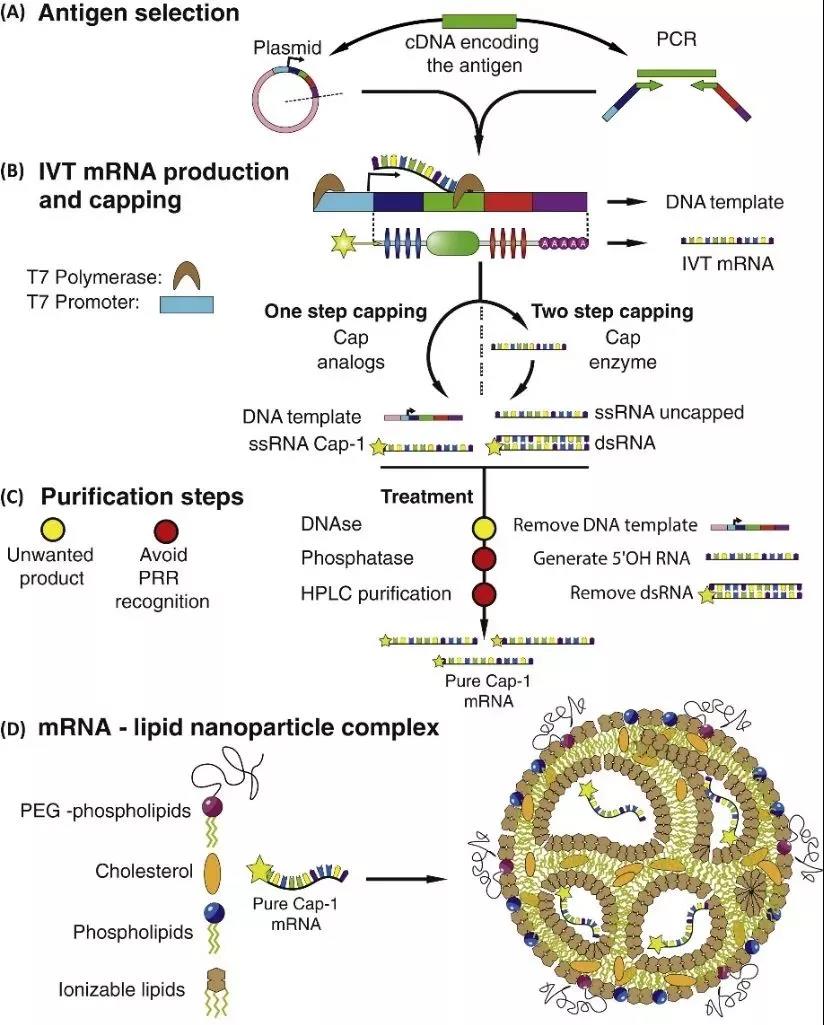
Obrázok 4: In vitro transkripčný (IVT) proces produkcie a zostavovania mRNA [5]
Príprava plazmidovej DNA vo veľkom meradle
Purifikácia plazmidovej DNA odstraňuje hlavne kontaminanty, ako je RNA, endotoxín DNA s otvoreným kruhom, hostiteľský proteín a hostiteľskú nukleovú kyselinu a zvyčajne transformuje rekombinantný plazmid na E. coli.E. coli prechádza fermentáciou s vysokou hustotou, potom separáciou tuhá látka-kvapalina a zberom E. coli.E. coli sa potom podrobí alkalickej lýze, odstredivej separácii tuhá látka-kvapalina a mikrofiltračnému čireniu po lýze, ultrafiltrácii a koncentrácii po vyčírení a potom chromatografickému čisteniu.

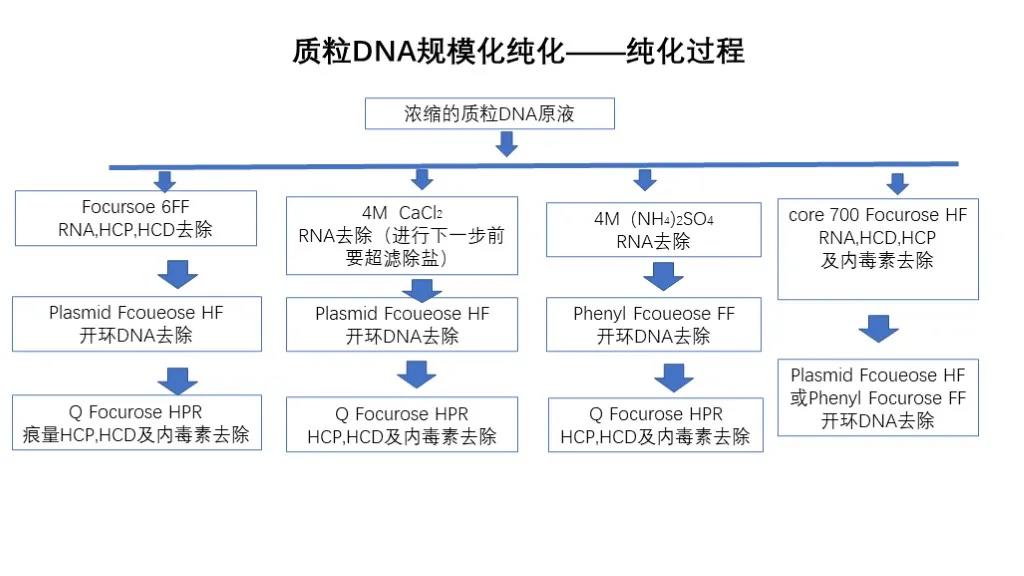
Purifikácia plazmidovej DNA:
Foregene General Plasmid Mini Kit
【1】苗鹤凡, 郭勇, 江新香.mRNA疫苗研究进展及挑战[J].免疫学杂志2016(05):446-449.
【2】Pardi N, Hogan MJ, Porter FW a kol.mRNA vakcíny – nová éra vo vakcinológii[J].Nature Reviews Drug Discovery, 2018.
【3】Kramps T., Elbers K. (2017) Úvod do RNA vakcín.In: Kramps T., Elbers K. (eds.) RNA Vaccines.Methods in Molecular Biology, zv. 1499. Humana Press, New York, NY.
【4】Maruggi G, Zhang C, Li J a kol.mRNA ako transformačná technológia pre vývoj vakcín na kontrolu infekčných chorôb[J].Molekulárna terapia, 2019.
【5】Sergio Linares-Fernández, Céline Lacroix, Prispôsobenie mRNA vakcíny na vyváženie vrodenej/adaptívnej imunitnej odpovede, Trendy v molekulárnej medicíne, zväzok 26, vydanie 3, 2020, strany 311-323.
Čas odoslania: august-05-2021








