1. Základné znalosti (ak chcete vidieť experimentálnu časť, preneste si ju priamo do druhej časti)
Ako derivačná reakcia konvenčnej PCR, Real time PCR hlavne monitoruje zmenu množstva amplifikačného produktu v každom cykle PCR amplifikačnej reakcie v reálnom čase prostredníctvom zmeny fluorescenčného signálu a kvantitatívne analyzuje východiskový templát prostredníctvom vzťahu medzi hodnotou ct a štandardnou krivkou.
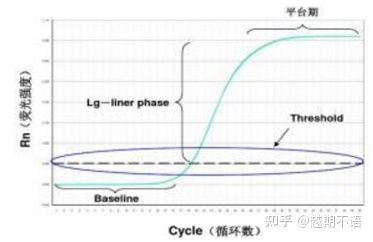
Špecifické údaje RT-PCR súzákladná línia, prah fluorescencieaHodnota Ct.
| základná línia: | Hodnota fluorescencie 3. – 15. cyklu je základná (základná), ktorá je spôsobená občasnou chybou merania. |
| Prah (prah): | Vzťahuje sa na limit detekcie fluorescencie nastavený vo vhodnej polohe v oblasti exponenciálneho rastu amplifikačnej krivky, vo všeobecnosti 10-násobok štandardnej odchýlky základnej línie. |
| Hodnota CT: | Je to počet cyklov PCR, keď hodnota fluorescencie v každej reakčnej skúmavke dosiahne prah. Hodnota Ct je nepriamo úmerná množstvu počiatočnej šablóny. |
Bežné metódy označovania pre RT-PCR:
| metóda | výhodu | nedostatok | pôsobnosť |
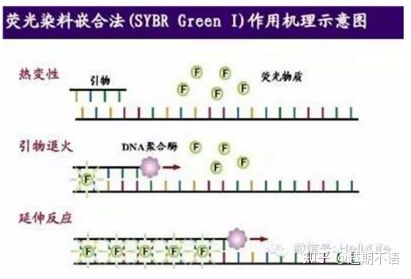
| Zelená SYBRⅠ | Široká použiteľnosť, citlivá, lacná a pohodlná | Požiadavky na primer sú vysoké, náchylné na nešpecifické pásy | Je vhodný na kvantitatívnu analýzu rôznych cieľových génov, výskum génovej expresie a výskum transgénnych rekombinantných zvierat a rastlín. |
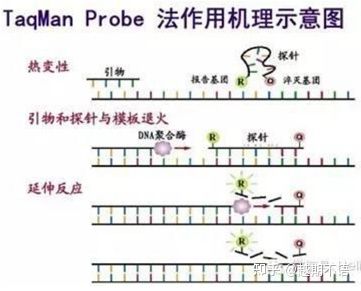
| TaqMan | Dobrá špecifickosť a vysoká opakovateľnosť | Cena je vysoká a vhodná len pre konkrétne ciele. | Detekcia patogénov, výskum génov rezistencie na lieky, hodnotenie účinnosti liekov, diagnostika genetických chorôb. |
| molekulárny maják | Vysoká špecifickosť, fluorescencia, nízke pozadie | Cena je vysoká, je vhodná len na konkrétny účel, dizajn je náročný a cena je vysoká. | Analýza špecifických génov, analýza SNP |
2. Experimentálne kroky
2.1 O experimentálnom zoskupení- v skupine musí byť viacero jamiek a musia existovať biologické opakovania.
| ① | Prázdne ovládanie | Používa sa na detekciu stavu rastu buniek v experimentoch |
| ② | Negatívna kontrolná siRNA (nešpecifická siRNA sekvencia) | Ukážte špecifickosť pôsobenia RNAi.siRNA môže vyvolať nešpecifickú stresovú reakciu pri koncentrácii 200 nM. |
| ③ | Kontrola transfekčného činidla | Vylúčte toxicitu transfekčného činidla pre bunky alebo účinok na expresiu cieľového génu |
| ④ | siRNA proti cieľovému génu | Znížte expresiu cieľového génu |
| ⑤ (voliteľné) | pozitívna siRNA | Používa sa na riešenie problémov experimentálneho systému a prevádzkových problémov |
| ⑥ (voliteľné) | Fluorescenčná kontrolná siRNA | Účinnosť bunkovej transfekcie možno pozorovať mikroskopom |
2.2 Zásady návrhu základného náteru
| Veľkosť zosilneného fragmentu | Výhodne pri 100-150 bp |
| Dĺžka základného náteru | 18-25 bp |
| Obsah GC | 30%-70%, najlepšie 45%-55% |
| Hodnota Tm | 58-60 ℃ |
| Sekvencia | Vyhnite sa nepretržitému T/C;A/G nepretržité |
| 3 koncová sekvencia | Vyhnite sa GC bohatému alebo AT bohatému;terminálna báza je výhodne G alebo C;najlepšie je vyhnúť sa T |
| Komplementárnosť | Vyhnite sa komplementárnym sekvenciám s viac ako 3 bázami v priméri alebo medzi dvoma primérmi |
| Špecifickosť | Na potvrdenie špecifickosti priméru použite vyhľadávanie výbuchom |
①SiRNA je druhovo špecifická a sekvencie rôznych druhov sa budú líšiť.
②SiRNA je balená v lyofilizovanom prášku, ktorý možno stabilne skladovať 2-4 týždne pri izbovej teplote.
2.3 Nástroje alebo činidlá, ktoré je potrebné pripraviť vopred
| Primer (interná referencia) | Vrátane dvoch vpred a vzad |
| Primery (cieľový gén) | Vrátane dvoch vpred a vzad |
| Cieľová Si RNA (3 prúžky) | Vo všeobecnosti spoločnosť syntetizuje 3 prúžky a potom si vyberie jeden z troch pomocou RT-PCR |
| Súprava na transfekciu | Lipo2000 atď. |
| Súprava na rýchlu extrakciu RNA | Na extrakciu RNA po transfekcii |
| Súprava rýchleho spätného prepisu | pre syntézu cDNA |
| PCR amplifikačná súprava | 2×Super SYBR Green qPCR Master Mix |
2.4 Pokiaľ ide o problémy, ktorým je potrebné venovať pozornosť v konkrétnych experimentálnych krokoch:
① proces transfekcie siRNA
1. Na nanesenie si môžete vybrať 24-jamkovú platničku, 12-jamkovú platničku alebo 6-jamkovú platňu (priemerná koncentrácia RNA navrhovaná v každej jamke 24-jamkovej platne je približne 100-300 ng/ul) a optimálna hustota transfekcie buniek je až 60 % - 80 % alebo tak
2. Kroky transfekcie a špecifické požiadavky sú prísne v súlade s pokynmi.
3. Po transfekcii je možné vzorky odobrať do 24-72 hodín na detekciu mRNA (RT-PCR) alebo detekciu proteínov do 48-96 hodín (WB)
② Proces extrakcie RNA
1. Zabráňte kontaminácii exogénnymi enzýmami.Zahŕňa to najmä prísne nosenie masiek a rukavíc;používanie sterilizovaných pipetových špičiek a EP skúmaviek;voda použitá v experimente musí byť bez RNázy.
2. Odporúča sa urobiť dvakrát, ako sa odporúča v súprave na rýchlu extrakciu, čím sa skutočne zlepší čistota a výťažok.
3. Odpadová kvapalina sa nesmie dotýkať kolóny RNA.
③ Kvantifikácia RNA
Po extrakcii RNA je možné ju kvantifikovať priamo pomocou Nanodrop a minimálna hodnota môže byť len 10 ng/ul.
④ Proces reverznej transkripcie
1. Kvôli vysokej citlivosti RT-qPCR by sa pre každú vzorku mali urobiť aspoň 3 paralelné jamky, aby sa zabránilo tomu, že následné Ct bude príliš odlišné alebo SD nebude príliš veľké na štatistickú analýzu.
2. Nezmrazujte a nerozmrazujte Master mix opakovane.
3. Každá hadička/otvor musí byť nahradený novým hrotom!Na pridávanie vzoriek nepoužívajte nepretržite rovnakú špičku pipety!
4. Film pripojený k 96-jamkovej platni po pridaní vzorky je potrebné uhladiť platňou.Pred umiestnením na stroj je najlepšie odstrediť, aby kvapalina na stene skúmavky mohla stekať dole a odstrániť vzduchové bubliny.
⑤ Spoločná analýza kriviek
| Žiadne obdobie logaritmického rastu | Možno vysoká koncentrácia šablóny |
| Žiadna hodnota CT | Nesprávne kroky na detekciu fluorescenčných signálov; degradácia primérov alebo sond – jej integritu možno detegovať PAGE elektroforézou; nedostatočné množstvo šablóny; degradácia šablón – zamedzenie vnášania nečistôt a opakovaného zmrazovania a rozmrazovania pri príprave vzoriek; |
| Ct > 38 | Nízka účinnosť zosilnenia;PCR produkt je príliš dlhý;rôzne zložky reakcie sú degradované |
| Lineárna krivka zosilnenia | Sondy sa môžu čiastočne znehodnotiť opakovanými cyklami zmrazovania a rozmrazovania alebo dlhodobým vystavením svetlu |
| Rozdiel v duplicitných otvoroch je obzvlášť veľký | Reakčný roztok nie je úplne roztavený alebo reakčný roztok nie je zmiešaný;termálny kúpeľ prístroja PCR je kontaminovaný fluorescenčnými látkami |
2.5 O analýze údajov
Analýza údajov qPCR sa dá rozdeliť na relatívnu kvantifikáciu a absolútnu kvantifikáciu.Napríklad bunky v liečenej skupine v porovnaní s bunkami v kontrolnej skupine,
Koľkokrát sa zmení mRNA génu X, to je relatívna kvantifikácia;v určitom počte buniek mRNA génu X
Koľko kópií je, to je absolútna kvantifikácia.Zvyčajne to, čo v laboratóriu používame najviac, je relatívna kvantitatívna metóda.zvyčajnemetóda 2-ΔΔctsa najviac používa v experimentoch, preto tu bude podrobne predstavená iba táto metóda.
Metóda 2-ΔΔct: Získaný výsledok je rozdiel v expresii cieľového génu v experimentálnej skupine v porovnaní s cieľovým génom v kontrolnej skupine.Vyžaduje sa, aby sa účinnosť amplifikácie cieľového génu aj interného referenčného génu blížila k 100 % a relatívna odchýlka by nemala presiahnuť 5 %.
Metóda výpočtu je nasledovná:
Δct kontrolná skupina = ct hodnota cieľového génu v kontrolnej skupine – ct hodnota interného referenčného génu v kontrolnej skupine
Δct experimentálna skupina = ct hodnota cieľového génu v experimentálnej skupine – ct hodnota interného referenčného génu v experimentálnej skupine
ΔΔct=Δct experimentálna skupina-Δct kontrolná skupina
Nakoniec vypočítajte násobok rozdielu v úrovni výrazu:
Zmeniť záhyb = 2-ΔΔct (zodpovedá funkcii Excel je POWER)
Súvisiace produkty:
Čas odoslania: 20. mája 2023